發布時間: 2016-10-21 瀏覽次數: 1547
醫藥網9月6日訊 9月2日,CFDA官網發布《關于化學藥品新注冊分類收費標準有關事宜的通告》(2016年第124號),對新分類后化學藥品注冊收費標準等有關事宜進行了明確:
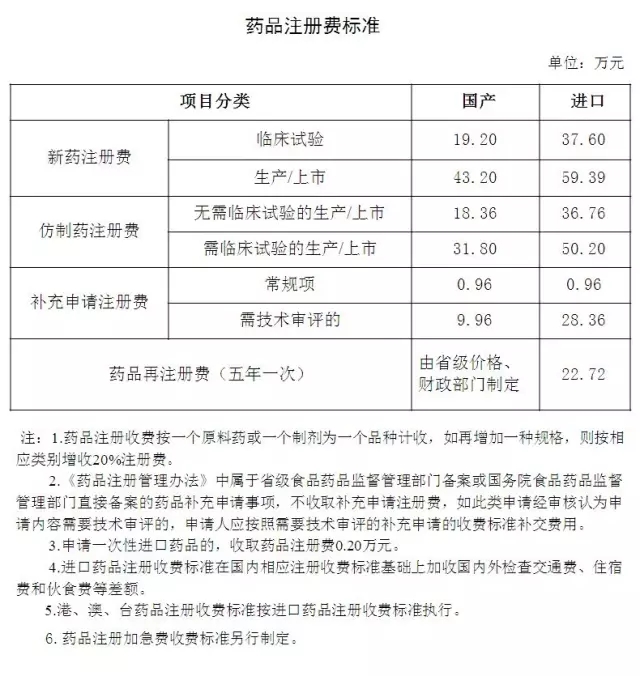
一、化學藥品新注冊分類1、2類別藥品的注冊申請,按照《關于發布藥品、醫療器械產品注冊收費標準的公告》(國家食品藥品監督管理總局2015年 第53號,以下簡稱2015年53號公告)中新藥注冊費標準收費;化學藥品新注冊分類3、4類別藥品的注冊申請,按照2015年53號公告中仿制藥注冊費標準收費。
其中,生產企業位于境內的,按照2015年53號公告中國產注冊費標準收費;生產企業位于境外的,按照2015年53號公告中進口注冊費標準收費。
二、化學藥品新注冊分類5類別藥品的注冊申請,按照2015年53號公告中進口無需臨床試驗的生產/上市、進口需臨床試驗的生產/上市注冊費標準收費。
三、《關于發布化學藥品注冊分類改革工作方案的公告》(國家食品藥品監督管理總局2016年 第51號,以下簡稱2016年51號公告)發布實施后,及本通告發布實施前,按照新注冊分類受理的但《行政許可項目繳費通知書》中適用收費標準與本通告不一致的,申請人于2016年10月30日前向原受理部門申請退還或補交相關費用。申請人需提交的材料包括:
(一)退費或補交費用申請;
(二)銀行匯款單據(復印件);
(三)《非稅收入一般繳款書》(申請補交費用時提供復印件,申請退費時提供原件);
(四)《藥品注冊申請表》(復印件);
(五)《受理通知書》(復印件)。
四、2016年51號公告發布實施前已受理,并申請按照新注冊分類進行審評審批的,申請人向原受理部門申請補交相關費用。申請人補交相關費用前,相應注冊申請的審評審批工作暫停。申請人需提交的材料包括:
(一)補交費用申請;
(二)銀行匯款單據(復印件);
(三)《非稅收入一般繳款書》(復印件);
(四)《藥品注冊申請表》(復印件);
(五)《受理通知書》(復印件)。
